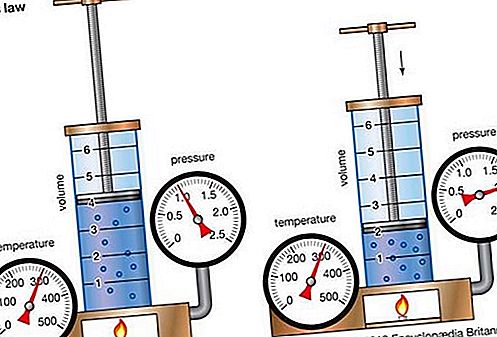
Boile likuma, ko sauc arī par Mariotte likumu, attiecības attiecībā uz gāzes saspiešanu un izplešanos pastāvīgā temperatūrā. Šis fiziķa Roberta Boila 1662. gadā formulētais empīriskais sakars norāda, ka dotā gāzes daudzuma spiediens (p) mainās apgriezti ar tā tilpumu (v) nemainīgā temperatūrā; ti, vienādojuma formā pv = k ir konstante. Attiecības atklāja arī franču fiziķis Edme Mariotte (1676).
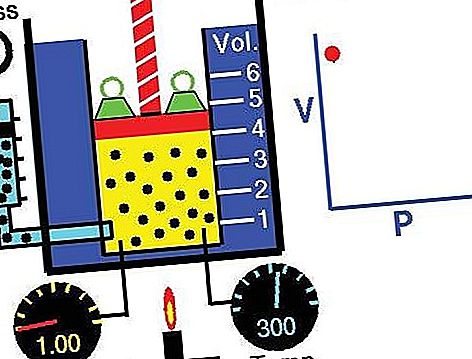
Likumu var atvasināt no gāzu kinētiskās teorijas, pieņemot, ka ir ideāla (ideāla) gāze (sk. Perfektu gāzi). Īstas gāzes ievēro Boilea likumu pie pietiekami zema spiediena, lai gan produkta pv parasti nedaudz pazeminās pie augstāka spiediena, kur gāze sāk atkāpties no ideālās izturēšanās.