Tehnēcijs (Tc), ķīmiskais elements, periodiskās tabulas 7. (VIIb) grupas sintētiskais radioaktīvais metāls, kas ir pirmais mākslīgi iegūtais elements. Izotopu tehnecijs-97 (4210 000 gadu pussabrukšanas periods) (1937. gadā) atklāja itāļu mineralogists Karlo Perjers un itāļu izcelsmes amerikāņu fiziķis Emilio Segrè molibdēna paraugā, kuru bija sabombardējuši deuteroni Berklijā (Kalifornijā). ciklotrons. Šis izotops ir visilgāk dzīvojošais kopums no tehnetija-85 līdz tehnetija-114, kas kopš tā laika ir ražots. Vissvarīgākais izotops, jo tas ir vienīgais, kas pieejams plašā mērogā, ir tehnecijs-99 (pussabrukšanas periods 211 000 gadu); tas tiek ražots kilogramos daudzumos kā kodoldalīšanās reakcijas kodolreaktoros. Metēla tehnēcijs izskatās kā platīns, bet parasti to iegūst kā pelēku pulveri. Tas kristalizējas sešstūrainā blīvi iesaiņotā struktūrā un ir supravadītājs zem 11,2 K. Ja nav tehnecija-99, tehnecija-97 un tehnecija-98 (4 200 000 gadu pussabrukšanas periods), tehnecija izotopi ir īslaicīgi. Metastable izotopu tehnecijs-99m (6 stundu pussabrukšanas periods), ko izmanto ar radiogrāfiskās skenēšanas ierīcēm, ir vērtīgs orgānu anatomiskās struktūras izpētei. Technecijs tiek izmantots arī kā metalurģijas marķieris un izstrādājumos, kas izturīgi pret koroziju.
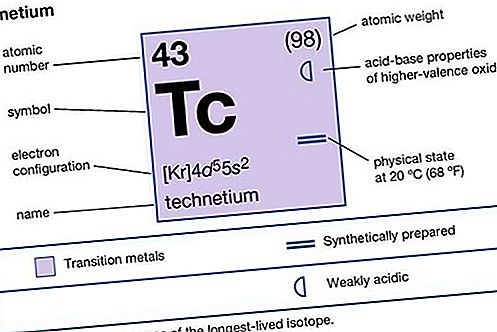
Tehnēcijs rodas Zemes garozā kā minimālas pēdas no urāna spontānās dalīšanās; salīdzinoši īsais pussabrukšanas laiks izslēdz jebkāda pirmatnējā tehnecija eksistenci uz Zemes. Amerikāņu astronoma Pola W. Merrila atklājums 1952. gadā, ka tehnecijs-99 atrodas S veida zvaigznēs, bija vērtīgs pierādījums par zvaigžņu evolūciju un nukleosintēzi. Tehnēcijs, ķīmiski līdzīgs rēnija (atomu numuru 75), pastāv oksidēšanas +7, +6, un +4 in savienojumus, piemēram, kālija pertehnāta, KTcO 4, Tehnēcija hlorīda, TcCl 6, un Tehnēcija sulfīds, TCS 2, attiecīgi. Savienojumi ir zināmi visos formālos oksidācijas stāvokļos no −1 līdz +7.
Elementa īpašības
| atomu skaitlis | 43 |
|---|---|
| visizplatītākais izotops | (99) |
| kušanas punkts | 2,172 ° C (3,942 ° F) |
| vārīšanās punkts | 4877 ° C (8,811 ° F) |
| īpaša gravitāte | 11,5 (20 ° C) |
| oksidācijas stāvokļi | +4, +6, +7 |
| elektronu konfigur. | [Kr] 4d 6 5s 1 |