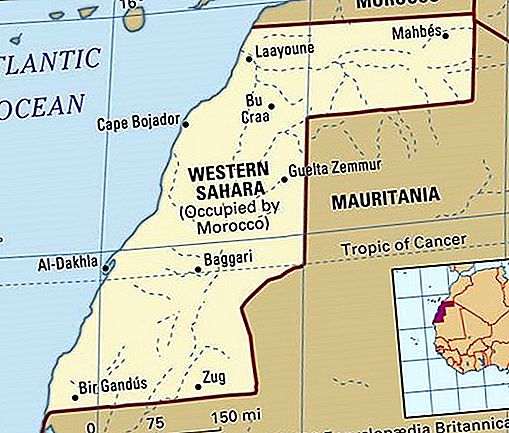
Konformācija - jebkurš no bezgalīgajiem iespējamiem atomu telpiskiem izvietojumiem molekulā, kas rodas, veidojot to atomu grupas rotācijas ap viengabalajām saitēm.
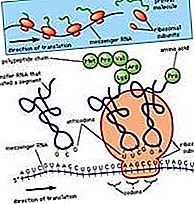
olbaltumvielas: olbaltumvielu konformācija saskarnēs
Tāpat kā daudzām citām vielām ar hidrofilām un hidrofobām grupām, šķīstošajiem proteīniem ir tendence migrēt gaisa saskarnē.
Jebkurai molekulai, kurā viena kovalenta saite savieno divas poliatomijas grupas, katrā no tām ir iespējamas dažādas konfigurācijas, katrā no tām vismaz viens atoms neatrodas gar attiecīgās vienotās saites asi. Vienkāršākā šāda molekula ir ūdeņraža peroksīds, kurā abas hidroksilgrupas var pagriezties viena pret otru ap skābekļa-skābekļa saites asi. Vairāk nekā vienas šādas vienas saites klātbūtne molekulā, piemēram, propāna (CH 3 ― CH 2 ― CH 3) klātbūtnē, tikai palielina situācijas sarežģītību, nemainot tās raksturu. Molekulās, piemēram, ciānūdeņraža (N≡C ― C≡N) vai butadiilēna (H ― C≡C ― C≡C ― H), visi atomi atrodas gar centrālās vienotās saites asi tā, ka nav atšķiramu konformāciju pastāvēt.
Kopumā katra atdalāmā molekulas uzbūve attēlo dažādas potenciālās enerģijas stāvokli, jo darbojas pievilcīgi vai atgrūdoši spēki, kas mainās atkarībā no attāluma starp dažādām struktūras daļām. Ja šie spēki nebūtu, visām pārvērtībām būtu tāda pati enerģija, un rotācija ap atsevišķo saiti būtu pilnīgi brīva vai neierobežota. Ja spēki ir spēcīgi, dažādas konfigurācijas enerģētikā vai stabilitātē ievērojami atšķiras: molekulā parasti būs stabils stāvoklis (viens ar zemu enerģijas līmeni) un tā pāreja uz citu stabilu stāvokli notiks tikai pēc tam, kad būs absorbēts pietiekami daudz enerģijas, lai sasniegtu un izietu cauri nestabilajai, kas iejaucas. uzbūve.
Piemēram, intramolekulārie spēki etānā ir tik vāji, ka to esamību var secināt tikai no smalkas ietekmes uz tādām termodinamiskām īpašībām kā entalpija un entropija. (Pat ja iekšējā rotācija etānā būtu stipri ierobežota, tā trīs visstabilākās konformācijas nav atšķiramas.) Atsevišķu sarežģītāku savienojumu molekulārās struktūras tomēr rada tik spēcīgus rotācijas šķēršļus, ka stereoizomērās formas - atšķirīgas tikai pēc uzbūves - ir pietiekami stabilas, lai būt izolētam.




![Ruanas kaujas franču vēsture [1418–1419] Ruanas kaujas franču vēsture [1418–1419]](https://images.thetopknowledge.com/img/world-history/2/battle-rouen-french-history-14181419.jpg)