Oglekļa nukleofilu pievienošana
Aldehīdiem pievieno plašu oglekļa nukleofilu daudzumu, un šādām reakcijām ir galvenā nozīme sintētiskajā organiskajā ķīmijā, jo produkts ir divu oglekļa skeleta kombinācija. Organiski ķīmiķi ir spējīgi samontēt gandrīz jebkuru oglekļa skeletu, lai cik sarežģīts tas būtu, atjautīgi izmantojot šīs reakcijas. Viens no vecākajiem un vissvarīgākajiem ir Grignarda reaģentu pievienošana (RMgX, kur X ir halogēna atoms). Franču ķīmiķis Viktors Grignards ieguva 1912. gada Nobela prēmiju ķīmijā par šo reaģentu un to reakciju atklāšanu.
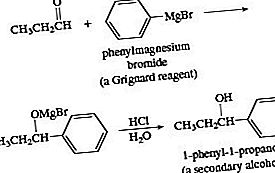
Grignarda reaģenta pievienošana aldehīdam, kam seko paskābināšana skābā ūdens vidē, dod spirtu. Papildinājums formaldehīdam dod primāro spirtu. Papildinot aldehīdu, kas nav formaldehīds, iegūst sekundāro spirtu.
Vēl viens oglekļa nukleofils ir cianīda jons, CN -, kas reaģē ar aldehīdiem, lai pēc paskābināšanas iegūtu ciānhidrīnus, savienojumus, kas satur OH un CN grupu uz tā paša oglekļa atoma.
Benzaldehīda ciānhidrīns (mandelonitrils) ir interesants ķīmiskās aizsardzības mehānisma piemērs bioloģiskajā pasaulē. Šo vielu sintezē milipedes (Apheloria corrugata) un glabā īpašos dziedzeros. Kad draud milipede, ciānhidrīns tiek izdalīts no tā uzkrāšanās dziedzera un notiek fermentu katalizēta disociācija, lai iegūtu cianīdūdeņradi (HCN). Tad milipede izdala HCN gāzi apkārtējā vidē, lai atvairītu plēsoņas. HCN daudzums, ko izstaro viena milipede, ir pietiekams, lai nogalinātu mazu peli. Mandelonitrils ir atrodams arī rūgtajās mandelēs un persiku bedrēs. Tās funkcija tur nav zināma.
Citas svarīgas reakcijas šajā kategorijā ir Knoevenagel reakcija, kurā oglekļa nukleofils ir esteris ar vismaz vienu α-ūdeņradi. Spēcīgas bāzes klātbūtnē esteris zaudē α-ūdeņradi, iegūstot negatīvi lādētu oglekli, kas pēc tam pievieno aldehīda karboniloglekli. Skābēšana, kam seko ūdens molekulas zudums, iegūst α, β nepiesātinātu esteri.
Vēl viena pievienošanas reakcija, kurā iesaistīts oglekļa nukleofils, ir Wittig reakcija, kurā aldehīds reaģē ar fosforānu (sauktu arī par fosfora ilīdu), iegūstot savienojumu, kas satur oglekļa-oglekļa divkāršo saiti. Wittig reakcijas rezultāts ir aldehīda karbonil skābekļa aizstāšana ar oglekļa grupu, kas piesaistīta fosforam. Vācu ķīmiķis Georgs Vittigs dalījās 1979. gada Nobela prēmijā ķīmijā par šīs reakcijas atklāšanu un tās izmantošanas attīstību sintētiskajā organiskajā ķīmijā.
Savienojumi, kas satur trimetilsililgrupu (―SiMe 3, kur Me ir metilgrupa, ―CH 3), un litija (Li) atoms uz viena un tā paša oglekļa atoma reaģē ar aldehīdiem tā dēvētajā Pētersona reakcijā, iegūstot tos pašus produktus, kas iegūst ar atbilstošu Wittig reakciju.
Nobīde pie α-oglekļa
α-halogenēšana
Α-ūdeņraža no aldehìdu var aizstāt ar hlora (Cl), broma (Br), vai joda (I) atoms, kad savienojums tiek apstrādāts ar Cl 2, Br 2, vai I 2, attiecīgi, vai nu bez katalizatora vai skāba katalizatora klātbūtnē.
Pēc tikai viena halogēna atoma pievienošanas reakciju var viegli apturēt. α-Halogenēšana faktiski notiek aldehīda enola formā (skatīt iepriekš aldehīdu īpašības: Tautomerisms), nevis pašā aldehīdā. Tāda pati reakcija notiek, ja tiek pievienota bāze, bet tad to nevar apturēt, kamēr visi α-halogēni, kas piestiprināti pie tā paša oglekļa, ir aizstāti ar halogēna atomiem. Ja ir trīs alfa-údeðraýa atomi pie viena oglekîa atoma, reakcija iet vienu soli tālāk, kā rezultātā tiek atšķelta X 3 C - jonu (kur X ir halogēna atoms) un veidošanās, ka sāls ar karbonskābi.

Šī reakcija tiek saukta haloforma reakcija, jo X 3 C - joni reaģē ar ūdeni vai sistēmā citā skābes Pašlaik ražot Savienojumu ar formāx 3 CH, kuras sauc haloforms (piemēram, CHCl 3 sauc hloroforma).




![Korfu Osmaņu un Venēcijas kara aplenkums [1716] Korfu Osmaņu un Venēcijas kara aplenkums [1716]](https://images.thetopknowledge.com/img/world-history/0/siege-corfu-ottoman-venetian-war-1716.jpg)
![Argentīnas Tucumán kongress [1816] Argentīnas Tucumán kongress [1816]](https://images.thetopknowledge.com/img/politics-law-government/1/congress-tucumn-argentina-1816.jpg)